據世界衛生組織的數字顯示,全球目前有逾5500萬人患有認知障礙,為第七大死因。本地研究指出,香港70歲以上人口有17%患有輕度認知障礙,患者當中有65%為阿茲海默症。
過去30年,阿茲海默症的治療主要循緩解症狀入手,卻未能延緩病情進展;隨著藥物研發技術及精準醫療的不斷進步,早期阿茲海默症的治療出現重大突破。現時已有新式抗類澱粉蛋白藥物可選擇性針對大腦中致病的類澱粉蛋白,從根源入手延緩病情惡化,有輕度認知障礙患者接受治療後可如常工作旅遊,維持現有認知功能。最新研究指出可提升患者至少3年獨立生活時間。
類澱粉蛋白代謝異常
腦神經專科黃家星醫生解釋,阿茲海默症的成因為類澱粉蛋白在大腦積聚,並形成斑塊,阻礙神經系統正常運作。「大腦中有一種稱為『類澱粉蛋白』的物質,能阻礙神經信號傳送,阿茲海默症患者的類澱粉蛋白由於腦內異常代謝作用,轉變成類澱粉蛋白斑塊並積聚腦中,逐漸引致腦萎縮。患者會喪失記憶力,並慢慢變痴呆,罪魁禍首正是這些不正常蛋白。」
類澱粉蛋白斑塊形成過程

早在阿茲海默症病發前10至20年,類澱粉蛋白可能已開始累積。斑塊累積會導致以下異常的腦部變化:
- 神經細胞受損
- 減低神經細胞功能及數量
- 腦萎縮及認知功能下降
黃醫生指:「阿茲海默症徵狀仍未表現出來的前10年,類澱粉蛋白已開始在腦內沉積;其後4年出現輕度認知障礙,患者有少許沒記性;然後進入早期阿茲海默症,患者無法處理複雜事情,工作或會受影響;中期則起居飲食、洗澡、穿衣也無法完成;後期則吞嚥亦有困難,整個過程或橫跨廿年。」
風險因素增致病可能
至於類澱粉蛋白這個「沉默殺手」到底從何而來?黃醫生表示現時醫學界仍未掌握,暫時只知道一些風險因素。「有極少數阿茲海默症是遺傳,即30、40歲已發病。最大風險因素是年齡及基因,然後是『三高』, 它會影響腦供血繼而影響認知功能;再來是腦儲備,就像銀行裡有多少存款,教育程度愈高,風險便愈低;還有缺乏運動,會減少腦部血液循環,影響腦細胞成長及發展;視力或聽力受損,或會加快大腦萎縮速度,這些都是阿茲海默症的危險因素。」
傳統治療針對徵狀緩解
正常人的大腦自40歲起便慢慢萎縮,屬正常衰老;但阿茲海默症患者的神經細胞及認知功能則快速下跌,引致症狀,而已沿用30年的兩類傳統藥物 ─ 膽鹼分解抑制劑及NMDA受體拮抗劑,便主要針對症狀緩解。「這類藥物稱為症狀緩解藥物,即紓緩性藥物,但因無法清除類澱粉蛋白,效用只能維持一時。即只能減輕病情,改善神經細胞的訊息傳遞,但減慢不了病情進展,未能從根源上治療阿茲海默症。」
新藥減慢病情進展
新式抗類澱粉蛋白藥物則能選擇性針對大腦中致病的類澱粉蛋白及去除神經毒性原纖維,減少其在腦中積聚,從根源入手延緩病情惡化。「新藥能用於治療阿茲海默症引起的輕度認知障礙及早期阿茲海默症,透過清除類澱粉蛋白,能減慢病情進展速度。臨床研究指出,68%患者在18個月內回復類澱粉蛋白陰性,表示與正常人數值相若且可延長獨立生活起碼三年。」
惟新藥的潛在風險,包括發燒、注射部位反應或類澱粉蛋白相關影像異常(ARIA)。
按時風險評估 亞洲人風險數據低
阿茲海默症患者本身亦會因為類澱粉蛋白在腦內沉積令血管破損、導致腦水腫及鐵質沉積等風險。而抗類澱粉蛋白藥物或有機會引致類似反應,但未必會有臨床症狀,治療前可透過ApoE4基因測試及按時進行磁力共振(MRI)管理及監察,以便及早掌握出現ARIA的風險。
「使用新藥治療的患者,會安排於第1、5、7及14次輸注前接受MRI檢查,以盡早發現ARIA。如沒發現ARIA,基本上往後出現的風險亦很低。目前我正在診治接受此藥物治療的二十多名病人中,平均年齡七十多歲,至今所有病人均未出現相關副作用。」
根據一項全球性雙盲對照臨床研究結果發現,在影像學及出現臨床症狀的風險管理,亞人的副作用風險較全球數據低。
真實個案 — 用藥後繼續工作
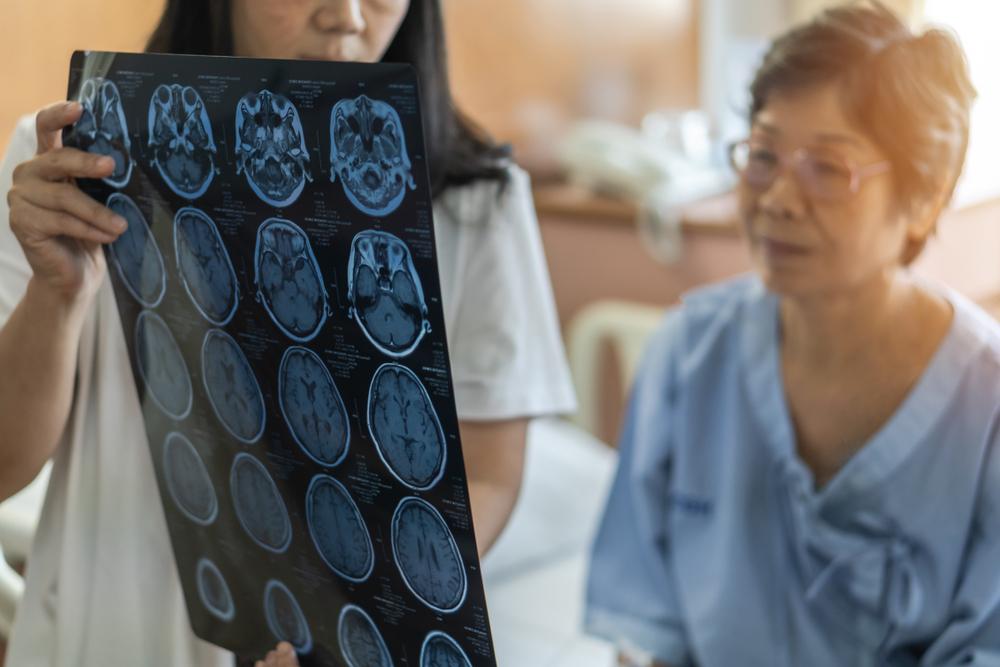
60歲的黃先生是位商人,一向精明能幹,最近卻突然記性轉差,常忘記東西放哪裡。太太覺得他有點異常,便帶他去求診。磁力共振影像掃描顯示他腦部開始萎縮,正電子斷層掃描更發現了腦中有異常蛋白,最終確診輕度認知障礙。
他獲處方新式抗類澱粉蛋白藥物,經9-10個月的治療後,認知狀態得以維持,可如常上班、洽談生意、旅行,處理銀行帳目、計劃、執行、決策上亦沒問題。
宜把握最佳治療時機
黃醫生表示:「新藥以用於輕度認知障礙患者的效果最好,尤其是高腦儲備即受高等教育者。反而阿茲海默症病情已屆中期、腦儲備不多者,成效便不大理想。」故想把握最佳治療時機,宜盡早發現病症並進行診斷。
藥物治療的同時,輔以非藥物治療方法,亦有助延緩阿茲海默症引起的認知衰退。「多用腦,例如打麻將、種花、養寵物、琴棋書畫、懷緬經歷等,總之別只坐着不動,要多刺激腦部活動,令現有神經細胞能建立新的神經連接,有助維持及提升認知功能。」
如何診斷阿茲海默症?
若醫生懷疑病人患有阿茲海默症,除臨床檢查外,還會安排認知能力評估測試,及透過影像測試排除與阿茲海默症相近的疾病。此外,可透過測試血液樣本中的生物標記,例如pTau217作症狀出現前作的診斷,並以正電子斷層掃描PET準確檢測患者腦中類澱粉蛋白的水平,以確診阿茲海默症。
5招預防阿茲海默症
雖然阿茲海默症的真正成因至今未明,但控制以下風險因素,可有助降低發病風險:
- 良好教育:維持規律的認知活動如閱讀書籍、報章、寫作等
- 保持良好視覺聽覺:如配戴老花眼鏡、助聽器,以改善視覺、聽覺上的不便。
- 恆常運動:包括進行體能運動如抗阻、帶氧運動,及腦部運動如打麻將、書法、畫畫等。
- 控制三高:如患有高血壓、高膽固醇或糖尿病,勿忘定時服藥及透過改善生活習慣控制。
- 健康飲食:「地中海式飲食」、「麥得飲食」的飲食模式如多進食蔬菜、魚類、少攝取紅肉,可有助預防腦退化。
- 註:本文原刊於第 175 期《Health Action 健康動力》,經黃家星醫生獲授權於 Bowtie 登刊。